
导语
①我国科学家在诱导性多能干细胞治疗重大疾病的研究中取得突破,首次利用干细胞再生疗法功能性治愈1型糖尿病;
②随着干细胞创新药政策持续催化,以及国内干细胞新药的申报审批等催化,国内干细胞创新药行业进入较好的投资阶段。
事件驱动
据媒体报道,我国科学家在诱导性多能干细胞治疗重大疾病的研究中取得突破,首次利用干细胞再生疗法功能性治愈1型糖尿病,该成果9月25日晚发表于国际权威期刊《细胞》。
行业透视
一、干细胞在再生医学与疾病治疗方面潜力巨大
干细胞在医学界被称为“万用细胞”,其是一类具有自我更新和多向分化能力的细胞,在特定的条件或者特定的信号诱导下能够分化成多种功能细胞或组织器官。干细胞疗法是指把健康的干细胞移植到患者体内,从而修复病变细胞或再建正常的组织。人源性干细胞及其衍生细胞治疗产品作为重要的再生医学产品,可能应用到几乎涉及人体所有重要组织器官的修复及研究人类面临的许多医学难题,在细胞替代、组织修复、疾病治疗等方面具有巨大潜力。
国内干细胞疗法相关指南适应症


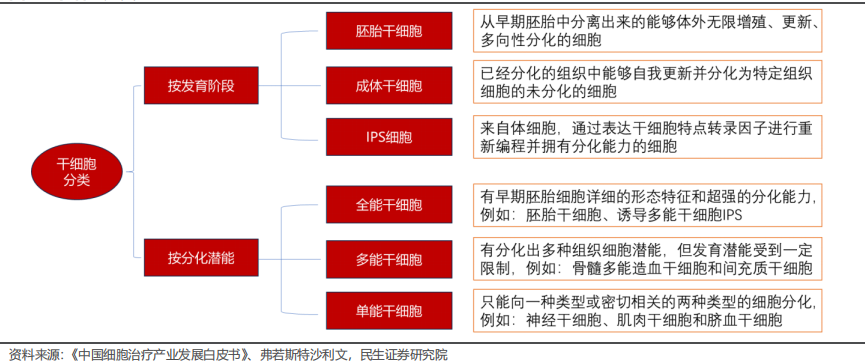
干细胞按分化潜能可以分为全能干细胞、多能干细胞以及单多能干细胞。在临床上较常使用的干细胞种类主要有间充质干细胞、造血干细胞、神经干细胞、皮肤干细胞、胰岛干细胞、脂肪干细胞等。长期以来造血干细胞移植一直是恶性血液肿瘤患者的主要治疗手段之一,但是在我国,造血干细胞被作为器官移植监管,而不是作为药物监管。间充质干细胞是我国目前干细胞临床研究中最多的一种,根据博雅干细胞的数据,截止2023年12月4号,我国共有127个干细胞研究备案项目,其中93个项目是间充质干细胞。
干细胞分类
二、全球范围内干细胞作为药品获批较少,国内已进入规范发展阶段
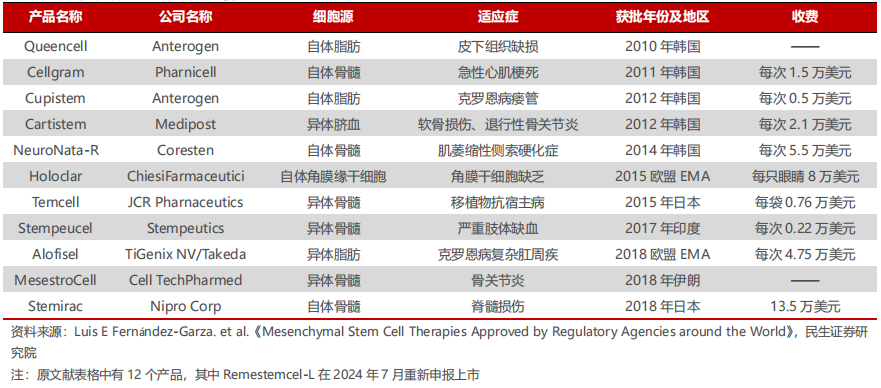
随着干细胞基础科研与临床转化的突破,国际上干细胞产品的监管经验逐渐丰富。根据同济大学附属东方医院干细胞转化医学产业基地国家干细胞转化资源库在“海南医学”上发表的一篇《全球干细胞临床研究现状与展望》的论文,全球在研干细胞临床千余项,但是干细胞创新药获批的较少。目前全球有11款干细胞药品获批上市,其中韩国5款、欧盟2款、日本2款,美国FDA至今未批准过一款(不包含造血干细胞)。
全球干细胞创新药获批情况
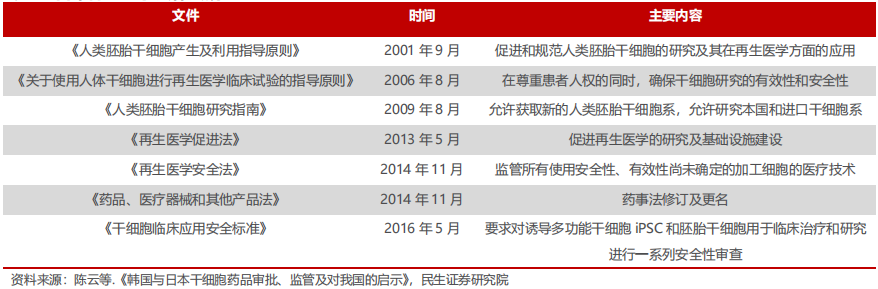
为了再生医疗产品的快速临床应用,日本建立了快速审批制度。2013 年日本先后颁布了《促进再生医疗安全并迅速推进法》、《再生医疗安全 确保法》和《医药品和医疗器械质量、有效性及安全性确保法》,大大缩短了再生医疗产品的审批时间,使日本成为最早将干细胞等再生医疗技术用于临床的国家。
日本再生医学法律法规
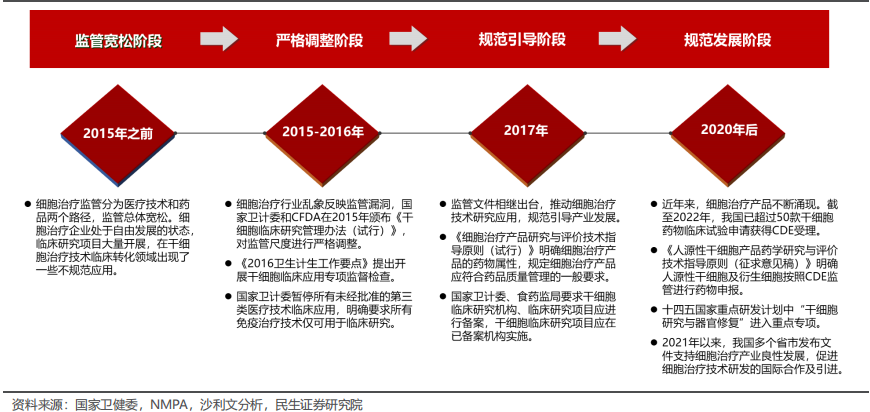
中国在细胞治疗方面的基础研究和临床试验开展较早,但是早期作为医疗技术服务监管较为宽松。2016年“魏则西事件”后,细胞治疗行业经历严格调整阶段,对于干细胞临床研究推进备案制度。到了2020年,CDE出台了多个干细胞创新药研发指南,引导国内干细胞按照创新药途径研发申报。
中国干细胞治疗相关监管发展历程
三、国内干细胞创新药迎来政策重大利好
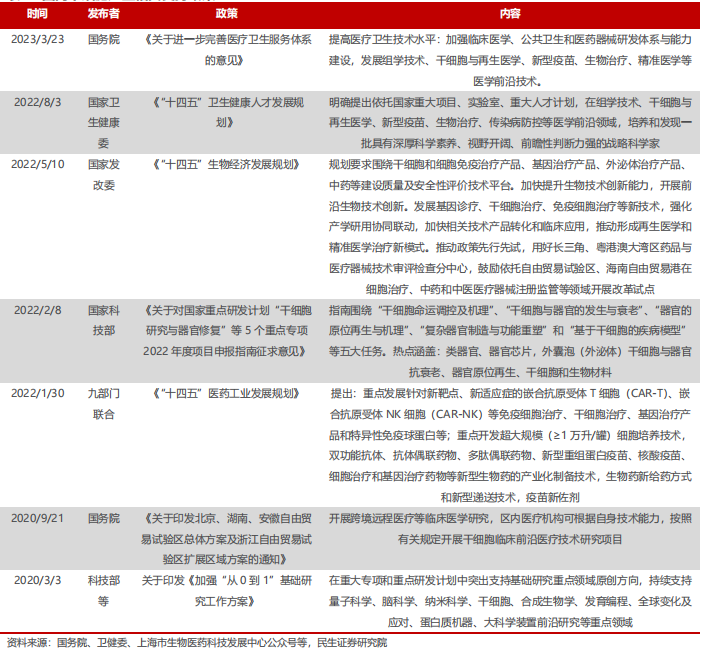
近年来国家重视细胞治疗产业的广阔应用前景,将其纳入生物医药领域重点 支持和发展的方向。国务院、国家科技部、国家发改委等均在多个政策文件中明确支持干细胞药物发展,北京、天津、湖南等各省市也出台了多项利好政策。
9月8日,商务部、国家卫生健康委、国家药监局发布关于在医疗领域开展扩大开放试点工作的通知,其中指出,自本通知印发之日起,在中国(北京)自由贸易试验区、中国(上海)自由贸易试验区、中国(广东)自由贸易试验区和海南自由贸易港允许外商投资企业从事人体干细胞、基因诊断与治疗技术开发和技术应用,以用于产品注册上市和生产。
国内干细胞产业相关支持政策
在国家和各地方鼓励干细胞产业发展的同时,CDE从2020年开始到目前,出台了大量的配套干细胞药物的技术指南,从干细胞药物临床前药学研究指南、临床研究指南、甚至聚焦干细胞具体适应症临床研究指南,给药企指明了干细胞药物申报途径及标准。
CDE发布的干细胞药物研发指南

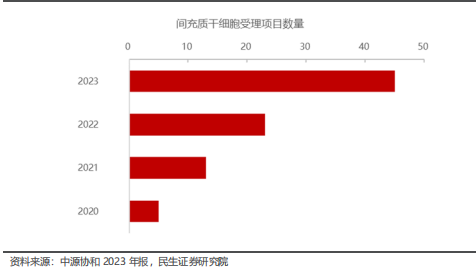
根据中源协和2023年报“2023年我国干细胞新药申报如火如荼,根据CDE官网查询全年获得受理的IND约45个,呈现逐年递增态势,截至2023年底,据不完全统计共获批约89个默示许可”。
2020-2023年底我国间充质干细胞IND情况
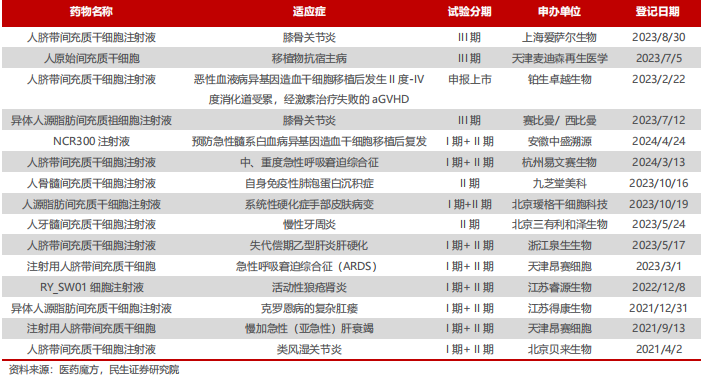
在目前我国近百个IND干细胞创新药中,据我们结合医药魔方数据不完全统计,处于III期临床试验约3项,II期临床试验约10项,适应症涉及关节、肺及呼吸疾病、抗宿主病、肝衰竭肝硬化、肛肠、脑卒中等多种疾病。
国内临床 II 期后干细胞创新药研发情况(不完全统计)
投资策略
中邮证券在研报中表示,近年来国家重视细胞治疗产业的广阔应用前景,将其纳入生物医药领域重点支持和发展的方向。在政策规范和技术获得突破性发展的节点来临下,真正具有技术和发展潜力的机构将成为在未来干细胞产业浪潮中的佼佼者,同时具有优秀上游干细胞存储资源的机构,也将快速向中下游药物研发和应用市场延伸,分享干细胞产业巨大市场。
民生证券在研报中指出,从2020年我国干细胞创新药规范发展开始,国内干细胞IND数量几乎每年翻一倍,到目前国内干细胞IND数量已近百,且其中有多款干细胞创新药进入了临床II期之后的研发阶段;2024年6月,铂生卓越的“艾米迈托赛注射液”成为全国首款获药监局上市申请受理的干细胞创新药。随着干细胞创新药政策持续催化,以及国内干细胞新药的申报审批等催化,国内干细胞创新药行业进入较好的投资阶段,建议关注拥有临床阶段干细胞创新药管线的公司。
个股关注
1、中源协和:国内最早全产业链布局干细胞技术的企业之一
①公司历来重视干细胞临床应用研发,在与医疗机构合作的备案项目方面,公司及下属企业、参股公司已完成 9 个国家卫健委和中央军委后勤保障部干细胞临床研究项目备案;
②公司干细胞创新药多适应症进临床,参股公司三有利和泽的牙髓干细胞Ⅱ期临床于2023年5月开始。
2、我武生物:脱敏治疗行业龙头
①子公司我武干细胞持续开展干细胞领域的研究开发,完成了自研完全培养基、分化培养基(成脂、成骨、成软骨)的开发;
②公司产品黄花蒿滴剂市场逐步上量,竞争格局良好,是国内唯一批准上市的黄花蒿脱敏治疗产品。
3、天士力:现代中药研发龙头
①公司以现代中药、化学药、生物创新药的丰富药品组合,突破性再生医学及4D整合健康管理解决方案,覆盖健康里程中的预查、预警、预防、诊断、治疗、康复等所有环节。
②2024年1月,公司人脐带间充质干细胞注射液(B2278 注射液)获得国家药监局的药物临床试验批准通知书。
风险提示
干细胞创新药研发风险,干细胞新药推广风险,行业政策变动风险,干细胞技术快速迭代风险,竞争加剧风险。
资料参考
20240925-民生证券-干细胞行业深度:国内外催化不断,干细胞创新药迎来风口。
20240512-中邮证券-医药生物行业周报:医药生物行业报告合成生物学和干细胞投资主题进一步推动医药板块投资升温。
免责声明
九方智投-投顾-杨建波-登记编号:A0740623090005;以上代表个人观点,仅供参考,不作为买卖依据,据此操作风险自担。投资有风险,入市需谨慎。













